
Em 2007, aos 33 anos e com seu pós-doutorado em Cirurgia Robótica no Children’s Hospital da Harvard Medical School recém-concluído, Carlo Camargo Passerotti retornou de Boston para São Paulo.
Sua especialização e seu objeto de estudo ainda não valiam muito por aqui, porque não havia no país nenhum robô com o qual ele pudesse operar. Mas ele sabia que era questão de tempo.
No ano seguinte, o país recebeu seu primeiro Da Vinci, uma máquina gigante, que custa um punhado de milhões de dólares e com quatro braços para realizar procedimentos microinvasivos. E o bauruense Carlo era o único médico capacitado para fazer isso.
“Na época não tinha treinado para operar. O único era eu”, relembra.
O urologista formado pela Universidade Federal de São Paulo, com mestrado e doutorado em biologia molecular, resolveu (assim como os irmãos) ser médico seguindo os passos do pai, um oftalmologista.
Enveredou pelo caminho da pesquisa em biologia molecular e desenvolveu um método de diagnóstico de câncer de bexiga que, segundo ele, é um dos melhores e mais eficientes que existem. Mas, até hoje, o teste não saiu do laboratório “por causa da política nacional”.
A linha de pesquisa o dirigiu para a especialização em urologia. Hoje coordenador do Centro Especializado em Urologia e do Centro de Cirurgia Robótica do Hospital Alemão Oswaldo Cruz, Carlo é também professor e médico assistente da disciplina de Urologia da Faculdade de Medicina da Universidade de São Paulo.
Neste “10 Perguntas para o Profissional”, ele conta um pouco mais sobre sua trajetória, os novos robôs que devem chegar ao mercado, as drogas promissoras para tratamento do câncer de próstata e conta por que a pandemia agravou os casos da doença no país.
Como você se tornou especialista em Urologia e em Cirurgia Robótica?
Sou do interior de São Paulo, de Bauru. Meu pai é médico, oftalmologista, é extremamente apaixonado pelo que ele faz. Ele tem 78 anos e até hoje trabalha de segunda a sábado. Desde meus 7 anos de idade sempre falei que queria fazer medicina. Entrei na Escola Paulista de Medicina da Universidade Federal de São Paulo, uma faculdade extremamente importante na área de pesquisa. Logo no começo vi uma palestra com a professora Helena Bonciani Nader, titular da biologia molecular e mulher do hoje falecido professor Carl Peter Von Dietrich, médico e presidente de associações de pesquisa. Ela não recebia alunos do primeiro ano para pesquisa, mas fui tão chato que fui aceito. Fiquei seis anos fazendo pesquisa em biologia molecular.
Em 1998, criei um método de diagnóstico de câncer de bexiga, que é um dos melhores que existem e, infelizmente, não saiu do laboratório até hoje.
No terceiro ano, me aceitaram para dar plantão voluntário num hospital em Osasco. O que o aluno de medicina quer é botar a mão na massa, ver paciente, operar. Foi quando resolvi fazer cirurgia geral. E urologia acabei fazendo por causa do meu trabalho de pesquisa com câncer de bexiga. Enquanto fazia residência em cirurgia geral, defendi mestrado com meu método. Na urologia, defendi doutorado junto com a residência. E meu sonho era fazer pós-doutorado fora.
Acabei indo para Harvard, fiquei dois anos e meio fazendo pós-doutorado em robótica. Nem se falava de robô no Brasil porque o custo era muito alto.
Até brincavam comigo, perguntando se eu ia trazer um robô no meu container. Lá, tinha emprego, estava contratado, mas resolvi voltar. Não ia competir de igual para igual porque era estrangeiro. E aqui eu já conhecia as pessoas. Voltei em setembro de 2007 e o robô chegou em março de 2008 para a primeira cirurgia. Na época, eu era o único treinado para operar o robô.
Como é esse teste para detecção de câncer de bexiga que você criou e por que ele não está no mercado?
É tipo o teste Elisa do HIV, mas ele detecta os níveis de ácido hialurônico na urina. Quando tem muito, é praticamente certo que ela tem ou vai ter um câncer de bexiga ou no trato urinário. Mas a política de investimento privado na universidade é tão esdrúxula que não se consegue trazer dinheiro de fora para investir ou comprar um método porque a faculdade não tem como receber esse recurso. É um negócio muito absurdo.
Em Harvard tem um escritório imenso, de cinco andares, só para cuidar de patente.
Você vai dar uma aula sobre algo que é uma novidade e é só ligar no escritório que já é orientado sobre o que você pode falar, o que não pode, o que tem que fazer para garantir que a patente seja sua. Aqui não tem nada disso, então você não tem apoio para a venda, não tem apoio para nada. Além de dar dinheiro para a faculdade, era algo que poderia ajudar muito a população. Hoje, o que existe, são testes que identificam o câncer bem no início, mas não há nada preventivo. A citologia oncótica, que colhe urina para ver se há células de câncer nela, falha em 20 a 30% dos casos. E esse método tinha sensibilidade na base de 90%.
Agora você continua trabalhando com pesquisa?
Quando eu voltei dos EUA, acabei fazendo livre docência na USP. Hoje, sou professor livre docente e participo da pós-graduação de lá. Então tenho orientandos e a gente faz pesquisa vendo viabilidade, treinamento em cirurgia robótica, a parte de biologia molecular e trabalhamos também com marcadores para câncer. Tenho alunos de pós graduação que estão fazendo essas pesquisas agora.
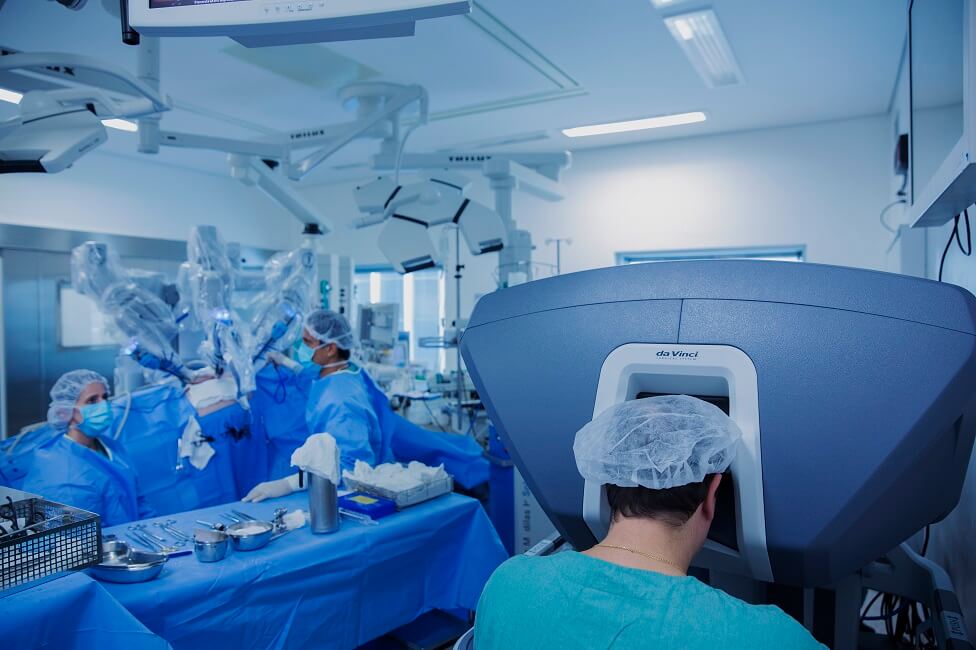
E como um robô ajuda uma cirurgia a ser mais precisa?
Ele é uma máquina enorme que pesa, se não me engano, uma tonelada e meia. Tem quatro braços nos quais se colocam três instrumentos mais a câmera do robô – e você controla isso.
Quando a gente fala em robô as pessoas pensam numa coisa que mexe sozinha, que fala, que pensa, e não tem nada a ver.
Tanto que se discute se o termo robô é adequado, porque é um sistema automatizado, que replica o seu movimento. O que eu faço, ele replica com mais firmeza, mais delicadeza. E tem uma escala. Se eu mexo 3 centímetros, ele mexe 1, com muita precisão. Ele tem também filtro de tremor, imagem 3D, então se consegue profundidade. Ele aumenta a imagem em 10 a 15 vezes.
O robô oferece várias vantagens e muito valor numa cirurgia delicada como a de câncer de próstata.
Tirar a próstata é fácil, qualquer um vai lá e faz isso. O problema é tirar e preservar o que tem em volta, preservar a potência, a continência. Eu preciso tratar o paciente, só que preciso também manter a qualidade de vida do paciente. O robô faz qualquer cirurgia dentro do abdômen e do tórax, por exemplo. Uma das desvantagens que ainda existe no Brasil, que não existe fora, é custo. O convênio não paga cirurgia robótica e paga laparoscopia. E o paciente que vai se submeter à cirurgia robótica tem que pagar os instrumentos do robô, o material do robô que é descartável, que é jogado fora depois. Hoje isso gira em torno de R$ 3 mil a R$ 5 mil, dependendo da cirurgia. Hoje em dia há 75 robôs no Brasil – ainda longe dos Estados Unidos, onde existem mais de 3.500.
O que hoje é o tema mais quente na cirurgia robótica?
O que vai acontecer agora é o surgimento de novos equipamentos, novos robôs, com novas tecnologias.
Alguns robôs já devem chegar no mercado no prazo de dois, três anos, aliados a inteligência artificial.
Ele vai ajudar a guiar a cirurgia, saber se o cirurgião está operando bem ou não está, diminuir erro. Tem quase 15 empresas pesquisando isso para trazer esses novos equipamentos. Eles também devem vir aliados a marcadores. Hoje temos um marcador apenas, de fluorescência. Quando esse marcador chega em um determinado local, aquele lugar fica com uma cor diferente, e é possível detectá-lo com mais precisão, para saber o que é preciso tirar na cirurgia.
Além disso, há um teste lançado recentemente para o câncer de próstata, o CT com PSMA, que é uma revolução.
Ele é um marcador na membrana da célula prostática, que gruda na célula. Então o paciente faz uma tomografia de corpo inteiro junto com uma cintilografia e é possível ver certinho se ele tem alguma lesão, se tem metástase. O PSMA vai revolucionar o diagnóstico e o tratamento. Existe um tratamento no qual se marca o PSMA com uma substância radioativa e injeta isso no paciente. Ele vai até a célula de câncer de próstata, que é atraída por ele, e mata a célula sem matar as outras. A grande revolução é isso eliminar a necessidade da quimioterapia mais para frente. Quimioterapia, do jeito que a gente conhecia, vai acabar. Porque o quimioterápico não mata só a célula de câncer, ele mata a boa também.
E há novas drogas que chegaram ao mercado brasileiro para ajudar na urologia?
Sim, tem diversas drogas que são bloqueios hormonais mais potentes para pacientes com câncer de próstata. Na verdade, o paciente que passa por um tratamento de câncer de próstata imagina que vai fazer quimioterapia.
Mas o tumor de próstata não responde muito à quimio, e sim mais à hormonioterapia.
Quando você bloqueia a testosterona, mata o tumor ou inibe ele de crescer. A comparação, que não é muito semelhante, mas funciona para entender, é pensar em uma infecção de urina. Imagine que o paciente toma um antibiótico e, de 100 bactérias, duas são resistentes a ele. Assim, 98 são mortas, mas duas vão crescer e o paciente vai ficar com uma infecção resistente. A células de câncer são um pouco assim. Dou um remédio forte que mata 98, mas dou espaço para as outras duas crescerem e ficarem resistentes. Esses hormônios então são para tentar matar essa célula que a gente não conseguiu matar com os hormônios antigos. Tem a enzalutamida, a abiraterona, a apalutamida, há várias linhas desses hormônios. Eles são extremamente caros, R$ 15 mil, 20 mil por mês de tratamento, mas alguns convênios pagam.
Qual é o principal problema a ser solucionado na saúde do brasileiro na sua área?
Do homem brasileiro é o câncer de próstata, com certeza. E este novembro é especial, porque a gente deixou de fazer check-up – e o câncer de próstata só é diagnosticado quando se faz check-up. Recebo diversas piadinha sobre o check-up. Uma delas diz que o homem inventou o raio X, a tomografia, mas não inventou exame melhor para fazer o diagnóstico de câncer de próstata do que o toque. O fato é que não existe nada melhor ainda do que o PSA e o toque.
Para se fazer o diagnóstico em massa, é preciso ser um teste barato e fácil. E o PSA e o toque são assim.
A ressonância, que pode ser equivalente ao toque, custa R$ 3 mil. Quando vou fazer uma ressonância de check-up? Nunca. Ainda tem muito preconceito com o exame, mas este ano teve um agravante: a pandemia e o pânico da população. No meu consultório, as consultas caíram 90% no começo da pandemia. As cirurgias também. Hoje, minhas consultas voltaram 90%.
Mas eu estou diagnosticando cânceres mais agressivos porque os pacientes deixaram de fazer check-up.
Das cirurgias, voltaram 30% a 40% só, porque para eu fazer o diagnóstico preciso do PSA e do toque. Então imagine que o paciente faz a ressonância e dá positivo. Depois faz a biópsia, que dá positivo. E tem que esperar dois meses para operar. O volume de cirurgias deve voltar só dentro de dois, três meses.
E agora, com o questionamento sobre essa onda de Covid de novo, não sei o que vai acontecer.
Pense em uma pessoa que devia ter feito no começo do ano seu check-up. Entrou a pandemia e ela não fez. Mas ela não está com isso atrasado seis meses ou oito meses, porque o último que ela fez foi no começo do ano passado. Por isso quando o diagnóstico é feito, o câncer já está mais agressivo, não tem jeito.
Como é a estrutura com a qual você trabalha no Oswaldo Cruz?
No Centro de Urologia agregamos diversos profissionais de vários setores. É possível fazer lá o tratamento completo não só de câncer, mas de litíase, de problemas de urologia feminina, urologia pediátrica, urologia geral. Tem também a parte multidisciplinar com fisioterapeuta, psicóloga.
O tratamento é bem humanizado, com profissionais de extrema qualidade.
Acredito que é um dos mais completos do Brasil. Já o Centro de Robótica é um dos pioneiros. O Oswaldo Cruz, o Sírio-Libanês e o Einstein foram os primeiros hospitais, em 2008, a comprar o robô. Já trocamos o nosso e estamos para trocar de novo. Esperamos o próximo modelo. O centro se diferencia sempre por buscar novas tecnologias. Trouxemos o PSMA e a ressonância multiparamétrica, que é a melhor que tem hoje em dia. Nosso diagnóstico de biópsia é uma novidade. Antes ela era feita de maneira aleatória, pegava-se tecido em qualquer lugar. Hoje é feita uma ressonância e, se uma lesão é encontrada, o ultrassom o guia, como um GPS, direto para a lesão. Tem lesões de 2mm que antigamente não se via.
Onde você acha que a robótica e a urologia vão estar em cinco ou dez anos?
Imagino que esse tratamento com PSMA e marcadores é a grande bola da vez. Acredito que tenha aberto uma porta para acabar com a cirurgia, acabar com tratamentos mais agressivos. Quando começamos algo na medicina, fazemos isso pelo fim da linha. Pegamos o paciente com o qual não há mais o que ser feito e testamos. E ele mostrou um resultado pequeno nessas pessoas.
Ou seja, mesmo naquele paciente que já não tinha mais expectativa nenhuma, ele mostrou um resultado de 15% a 30%.
Fico imaginando essas coisas quando são tratadas desde o início. É bem animador, um tratamento com pouquíssimo efeito colateral. Perde-se um pouco do olfato, do paladar, mas nada como o hormônio, que pode provocar impotência, ginecomastia, ganho de peso, aumento de risco cardiovascular e de morte.
Que notícia que você gostaria de ler em relação à saúde ou em relação à sua área?
A notícia que eu mais gostaria de ler é sobre a existência de um teste de sangue para diagnosticar qualquer câncer, principalmente o de próstata. Acho que esse é o desejo de todo homem. E estou falando como homem, não só como médico [risos].
